EN
欧盟 • MDR/IVDR合规导航

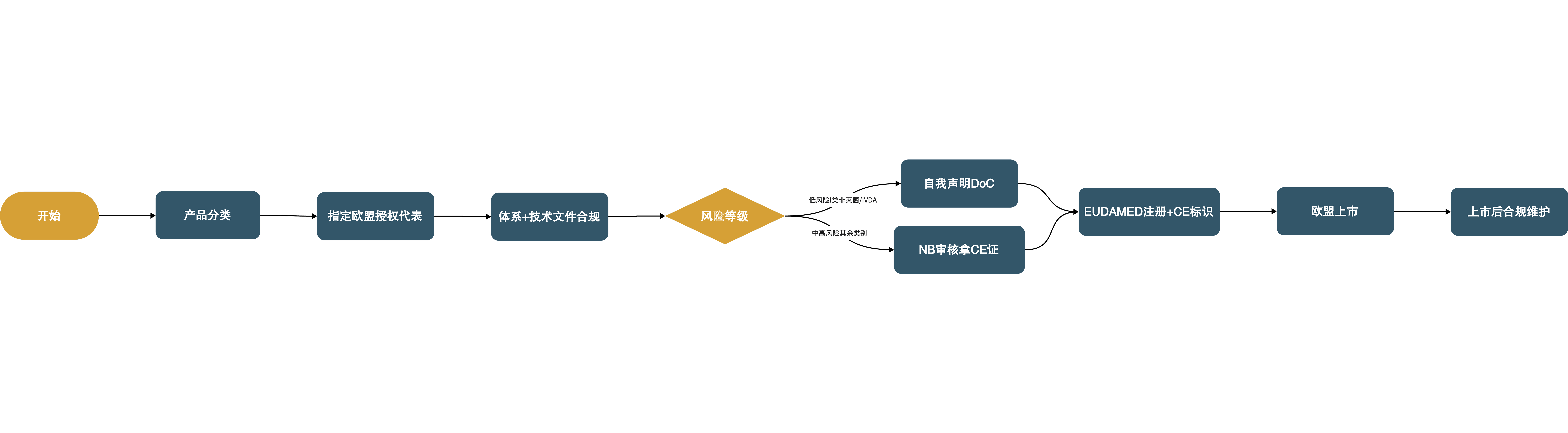
欧盟依托MDR(医疗器械)、IVDR(体外诊断)法规实施监管,产品实行明确风险分级,医疗器械分I、IIa、IIb、III类,IVD分A、B、C、D类,境外厂商需提前指定欧盟授权代表。低风险产品可走自我声明快速路径,中高风险产品需通过公告机构审核获取CE证书,完成EUDAMED注册后即可上市流通。
ELMAS提供欧盟一站式准入合规服务,覆盖产品分类、欧代委任、技术文件编撰、NB审核对接及EUDAMED注册,精通MDR/IVDR要求,同步提供上市后合规运维,助力产品快速落地欧盟市场。



 俄罗斯
俄罗斯
 独联体国家
独联体国家
 中国
中国
 印度
印度
 巴西
巴西
 美国
美国
 加拿大
加拿大
 欧盟
欧盟
 新加坡
新加坡
 马来西亚
马来西亚
 韩国
韩国
 日本
日本
 澳大利亚
澳大利亚



