EN
巴西 • 一体化注册通道

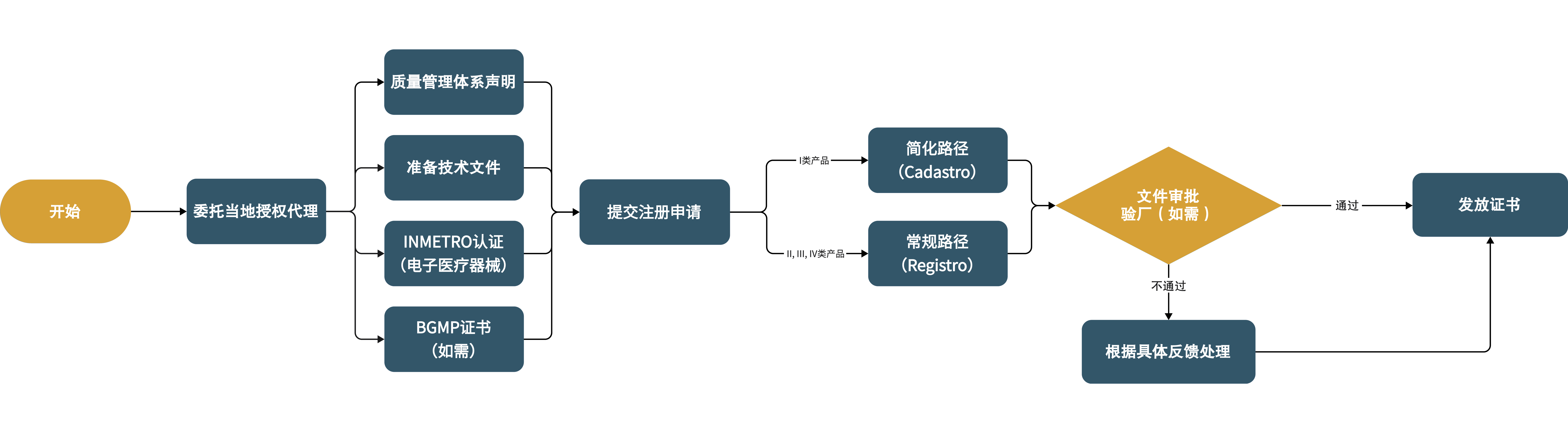
巴西医疗器械市场由ANVISA监管,产品按风险分为I-IV类,需进行完整注册。高风险设备还需接受GMP现场审核。
ELMAS团队能为您提供ANVISA注册的端到端服务。我们协助完成产品分类、葡萄牙语技术文档准备、测试协调和正式申请提交。我们的专家团队熟悉ANVISA的审评流程,能有效处理缺陷通知(Deficiency Notice)并提供专业回复。作为您在本地的巴代(LAR),ELMAS还负责GMP审核准备和上市后监管。凭借在巴西市场的丰富经验,我们帮助您高效应对ANVISA的严格要求,缩短注册周期,确保产品顺利进入这一拉丁美洲最大医疗市场。



 俄罗斯
俄罗斯
 独联体国家
独联体国家
 中国
中国
 印度
印度
 巴西
巴西
 美国
美国
 加拿大
加拿大
 欧盟
欧盟
 新加坡
新加坡
 马来西亚
马来西亚
 韩国
韩国
 日本
日本
 澳大利亚
澳大利亚



